Dr. Mario Nicolosi Specialista in Ortopedia e Traumatologia Specialista in Fisiatria
Metastasi ossee
Le metastasi ossee meritano un trattamento a parte rispetto alle altre metastasi sia per la loro alta frequenza che per le loro caratteristiche cliniche e le esigenze terapeutiche.
Patogenesi
Le metastasi sono riproduzioni a distanza del tumore originario: da questo tumore alcune cellule si staccano e migrano in una nuova sede ossea. Per potersi insediare devono causare un rimaneggiamento del tessuto osseo. Per fare ciò favoriscono l’intervento degli osteoclasti ( cellule che erodono l’osso) che , non solo distruggono l’osso ma favoriscono anche la crescita tumorale. Non tutte le cellule che si staccano dal tumore primitivo riescono però ad insediarsi e a dare origine a metastasi Le metastasi possono però, una volta insediatesi, assumere delle caratteristiche diverse da quelle del tumore di partenza. Si dividono in osteolitiche ed in osteoaddensanti. Nelle prime è prevalente l’azione destruente dell’osso da parte degli osteoclasti. Nelle seconde prevale l’azione produttrice di osso da parte degli osteoblasti. In entrambi i casi l’osso è più fragile. Nel primo caso perché l’azione distruttrice degli osteoclasti erode l’osso rendendolo più sottile, più a rischio di fratture anche per piccoli traumi, potendo giungere sino alla sua rottura spontanea ( che viene definita “patologica” ). Nel secondo caso perché la nuova formazione di osso da parte degli osteoblasti è attuata in maniera molto disordinata, senza rispettare le linee di forza dell’osso ( attraverso le quali si scaricano le sollecitazioni ), rendendo così l’osso più fragile anche se apparentemente più addensato.
Diffusione
35000 sono i nuovi casi per anno riportati dalla AIOM (
Associazione Italiana di Oncologia Medica ) in Italia. Questo numero è
destinato ad aumentare se non altro per l’allungamento della vita dei
pazienti oncologici dovuto al miglioramento delle terapie. Più a lungo
vive il paziente e più grande è la probabilità di insorgenza di
metastasi ossee che sono le terze in ordine di frequenza dopo quelle
al polmone e al fegato. I meccanismi attraverso i quali le cellule
tumorali si staccano dal tumore e si riproducano a distanza non sono
ancora del tutto chiari. Possiamo però statisticamente dire quali sono
le caratteristiche che mediamente hanno maggiori probabilità di
produrre metastasi. Alcuni tumori come quelli della mammella,
prostata, rene, polmone e tiroide rappresentano un fattore di rischio
importante per l’insorgenza di metastasi. Altri fattori di rischio
sono dati dalla dimensione del tumore ( tumori grandi che hanno già
raggiunto i linfonodi vicini ) o dal grado elevato di aggressività.
Esistono anche altri fattori che influenzano l’insorgenza come
eventuali ostacoli che le cellule metastatiche trovano nel loro
cammino, dal microambiente che circonda il tumore, dalle condizioni
generali del paziente.
Nelle donne 80% delle metastasi è prodotto dai tumori della mammella e
del polmone. Negli uomini la maggior parte delle metastasi è prodotta
da tumori della prostata e polmone. Anche i tumori dell’utero e della
pelle come i melanomi, possono generare metastasi ossee.
La sede più frequente è la colonna vertebrale ma qualunque osso può
essere attaccato dalle metastasi .
Prevenzione
Non esiste purtroppo, sino ad oggi, la possibilità di evitare che un tumore metastatizzi nelle ossa. Quello che bisogna fare e che può aiutare moltissimo è la diagnosi precoce del tumore primitivo e i controlli continui e puntuali, che soprattutto per quei tumori che metastatizzano più frequentemente come quelli della mammella e della prostata, possono portare ad una diagnosi e ad una cura precoci.
Sintomatologia
I sintomi sono molto subdoli e poco frequenti nel periodo
dell’insorgenza delle metastasi. Solo in un secondo periodo la
sintomatologia diventa eclatante ( dolori, fratture ). Nel 75% dei
casi non esiste sintomatologia dolorosa. Le metastasi vengono scoperte
durante gli approfondimenti strumentali che vengono eseguiti per
studiare la patologia tumorale.
Nel 25% circa dei casi esistono gli “ eventi scheletrici correlati “ :
una serie di sintomi e segni che portano a focalizzare l’attenzione
sull’apparato scheletrico. Il dolore osseo è il primo di questi segni:
è un dolore all’inizio saltuario, incostante che però, con l’avanzare
della malattia, peggiora , diventa continuo se non costante, senza
remissione neanche durante il riposo. Coll’avanzare della grandezza di
queste localizzazione secondarie l’osso si indebolisce, diviene più
fragile ed diviene a rischio di fratture. Le più frequenti sono quelle
a carico della colonna vertebrale ma non sono risparmiati neanche
quelle a carico degli arti.
Quando queste localizzazioni colpiscono la colonna vertebrale possono
provocare delle compressioni sul midollo nervoso provocando disturbi
neurologici importanti sia a livello degli arti ( disturbi della
motilità che possono giungere alla paralisi ) che a livello di vescica
e intestino ( incontinenza urinaria ed intestinale). L’invasione delle
cellule tumorali a livello del midollo osseo rosso può provocare
disturbi dell’emopoiesi ( cioè della formazione e della maturazione
delle cellule del sangue ) sin ad arrivare alla pancitopenia (
riduzione, cioè, di tutte le cellule del sangue ). Altri problema,
dovuti alla presenza di metastasi che demolendo l’osso riversano nel
sangue grandi quantità di calcio ) sono, la nausea, la perdita di
appetito, l’astenia , sino al coma.
Diagnosi
L’insorgenza di sintomatologia che possa far sospettare la presenza
di metastasi ossee e i controlli che devono essere eseguiti quando si
ha in trattamento un tumore mettono in atto controlli diagnostici che
si avvalgono di numerosi strumenti. Innanzitutto le “ comuni “
radiografie, la scintigrafia ossea che mette in evidenza le zone di
rimaneggiamento osseo per mezzo di un tracciante radioattivo, La TAC
molto utile per quantificare e studiare la grandezza delle metastasi e
la possibile invasione dei tessuti adiacenti, La Risonanza magnetica
che studia bene il midollo spinale, La PET che evidenzia molto bene,
in aggiunta alle altre, le lesioni da mieloma multiplo .
Anche gli esami di laboratorio devono essere messi in campo per
controllare i livelli di calcio e di fosfatasi alcalina ( di solito in
aumento ) nel sangue, i livelli di N-telopeptide nelle urine.
Infine la biopsia ossea deve essere eseguita per tipizzare bene la
metastasi per eseguire una terapia mirata.
Terapia
I pazienti affetti solo da metastasi ossee hanno una sopravvivenza
più lunga rispetto a pazienti affetti da metastasi anche in altri
organi . Col passare del tempo possono sopravvenire le complicanze
scheletriche di cui abbiamo parlato prima ( compressioni midollari,
fratture, dolori ) .
Il trattamento si prefigge di rallentare/arrestare la crescita delle
cellule metastatiche con lo scopo di: lenire il dolore, evitare le
complicanze scheletriche ottenendo così una miglioramento della
funzionalità con contemporanea riduzione dell’invalidità del paziente
e miglioramento del la qualità della vita.
Il tipo di trattamento da mettere in atto deve tenere conto di diversi
parametri come il tipo di tumore primitivo, la sede delle metastasi,
il numero di ossa colpite, le condizioni generali del paziente.
Naturalmente vi è anche un trattamento per le eventuali fratture
secondarie alle metastasi. Oggi ci possiamo avvalere di numerose armi
per la lotta alle metastasi ossee.
I trattamenti sistemici validi in presenza di numerose metastasi a
diversa localizzazione e che prevedono l’utilizzo della chemioterapia
( sia specifica per le metastasi ossee che più generale per metastasi
in organi diversi ); della ormonoterapia ( particolarmente valida in
caso di tumori che si sviluppano con lo stimolo ormonale) che blocca
la produzioni degli ormoni responsabili dello sviluppo tumorale o
blocca l’azione degli ormoni sulle cellule neoplastiche;
l’immunoterapia ( che aiuta il sistema immunitario del paziente a
lottare contro le cellule tumorali; i radio farmaci ( che con la loro
componente radioattiva vanno a colpire le metastasi); i bifosfonati (
aiutano l’osso contro la distruzione da parte degli osteoclasti ); il
denosumab ( anticorpo monoclonale che blocca, con un sistema diverso
dai precedenti farmaci, l’azione degli osteoclasti rinforzando le ossa
).
I trattamenti locali si avvalgono di numerose metodiche. La
Radioterapia che ha lo scopo di ridurre la grandezza della massa e di
alleviare la sintomatologia dolorosa; l’ablazione che riesce a
distruggere il tessuto tumorale con diversi mezzi come il caldo o il
freddo; la chirurgia che deve intervenire o in caso di metastasi
uniche o in caso di ossa particolarmente deboli o dopo una frattura;
la vertebroplastica nel caso di tumori vertebrali,
L’elettrochemioterapia che ha un suo spazio dove hanno fallito le
altre terapie .
Elettrochemioterapia
L’elettrochemioterapia è il risultato della combinazione di due
effetti: la somministrazione di dosi ridotte di farmaco e
l’elettroporazione delle membrane cellulari.
L’elettroporazione delle membrane cellulari si ottiene con
l’applicazione locale di brevi e intensi impulsi elettrici che
permeabilizzano reversibilmente la membrana cellulare. Ciò agevola
l’ingresso nella cellula tumorale del farmaco ( generalmente non
permeante o scarsamente permeante ). In questa maniera viene
potenziato l’effetto citotossico del farmaco stesso ma limitatamente
ai tessuti esposti agli impulsi elettrici.
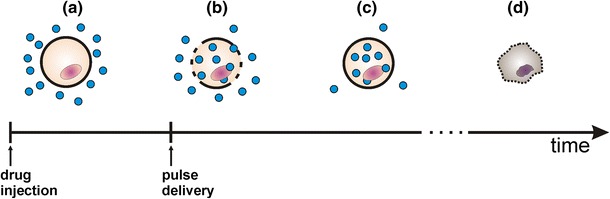
Fig. 1
L’elettrochemioterapia non è una tecnica nuova e in fase
sperimentale. Essa nasce da studi preclinici e clinici effettuati
negli ultimi 20 anni con l’approvazione di due progetti europei : Il
Clinoporator e l’Esope.
Il primo rivolto alla progettazione e costruzione di
un’apparecchiatura specificatamente dedicata all’applicazione
dell’elettrochemioterapia.
Il secondo è, come dice l’acronimo stesso, l’European Standard
Operating Procedure for Electrochemotherapy
Questi studi sono stati condotti dall’Istituto Gustave-Roussy di
Parigi, dal Cork Cancer Center in Irlanda, dall’Herlev Hospital di
Copenaghen, dall’Istituto di Oncologia di Lubiana.
Le indicazioni cliniche elettive dell’elettrochemioterapia riguardo
all’osso (esistono numerose indicazioni per altri tipi di tumore)
sono:
‐ Tumori dei tessuti molli difficilmente aggredibili con la chirurgia
‐ Metastasi ossee sintomatiche dello scheletro appendicolare
‐ Recidive in aree già in precedenza irradiate
I vantaggi sono numerosi e tra questi ne abbiamo sottolineato alcuni
che ci sembrano importanti:
‐ Durata della risposta locale in caso di risposta completa
al trattamento
‐ Capacità di lenire lesioni dolorose o sanguinanti
‐ Efficacia nel preservare l’estetica del paziente e le sue
interazioni sociali; la terapia non lascia cicatrici o altro segno
evidente nella zona trattata
‐ Efficacia nel preservare la funzionalità di un organo
‐ Dosi ridotte di farmaco somministrate al paziente
‐ Breve durata della sessione di trattamento
Il nostro Centro è dotato della più moderna macchina per
elettroterapia prodotta.
Questa consente quindi anche il trattamento delle lesioni ossee prima
non possibili.
Gli esprimenti nel ratto prima
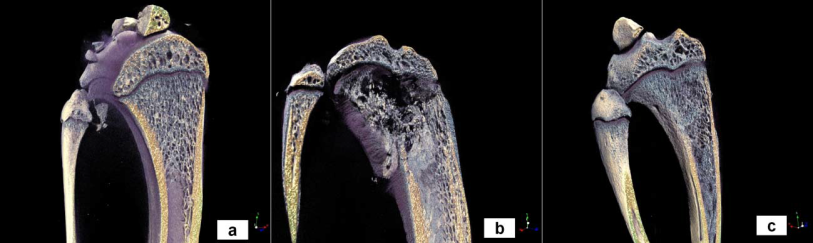
Fig. 2
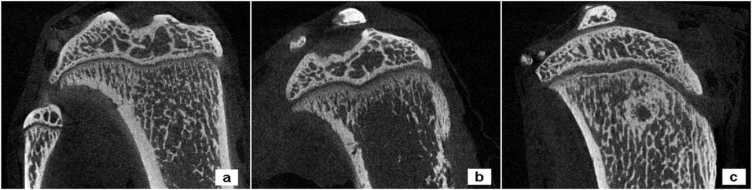
Fig. 3
e i trattamenti eseguiti su pazienti affetti da localizzazione ossee Fig. 4 Fig. 5 Fig. 6
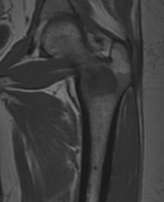

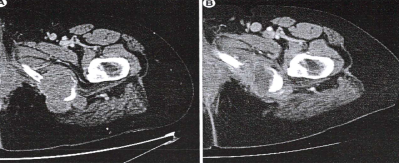
hanno permesso già di ottenere dei risultati confortanti per il trattamento delle metastasi ossee.
L’elettrochemioterapia viene praticata in ottantacinque Centri europei e in altri cinque Centri italiani.
Il Gruppo di studio SIOT (Società Italiana di Ortopedia e
Traumatologia) sulle metastasi ossee a messo a punto delle linee guida
per il trattamento delle metastasi ossee nello scheletro osseo degli
arti.
Le linee guida partono da una attenta classificazione delle metastasi
ossee che il Gruppo di Studio (del quale fa parte il Nostro Centro
Oncologico, ha cosi distinte
Classe 1: Pazienti con metastasi scheletrica solitaria da tumore
primitivo a buona prognosi (mammella, prostata, rene, tiroide) e con
prolungato intervallo libero da malattia ( > 3 anni ) dal tumore
primitivo alla metastasi
Classe 2: Pazienti con una frattura patologica nelle ossa lunghe
principali (omero, radio, ulna, femore e tibia)
Classe 3: Pazienti con una lesione a rischio di frattura patologica
nelle ossa lunghe principali:
a) Lesione litica della corticale ≥ 2,5
cm;
b) Distruzione della corticale ≥ 50% del
diametro
c) Dolore persistente o progressione
della lesione dopo radioterapia e/o chemioterapia
Classe 4:
1) Lesioni metastatiche osteoblastiche;
2) Lesioni osteolitiche o miste in ossa non
sottoposte a carico (ulna distale, coste, perone, clavicola);
3) Lesioni non a rischio di frattura nelle
principali ossa lunghe;
4) Lesioni per le quali l’unico intervento
possibile sarebbe l’amputazione dell’arto;
5) Lesioni nell’ala iliaca, arco pelvico
anteriore e scapola
(eccetto i pazienti inclusi nella classe 1)
Da questa classificazione scaturiscono queste linee guida
I pazienti delle classi 1, 2 e 3 ( le meno numerose ) devono essere
inviati in prima istanza al chirurgo ortopedico per il trattamento
chirurgico ed in seguito all’oncologo medico e/o al radioterapista per
le terapie adiuvanti.
I pazienti della classe 4 ( la più numerosa ) vanno trattati in prima
istanza con terapie non chirurgiche ( chemioterapia, radioterapia,
terapia ormonale, etc. ). Come primo trattamento si possono anche
adottare tecniche mini invasive in collaborazione tra i vari
specialisti ( Lesioni che mal rispondono a trattamenti chemioterapici
o radioterapici, pazienti già sottoposti a numerose radioterapie, etc.
)
In caso di fallimento meccanico ( frattura patologica o progressione
di malattia con lesione a rischio di frattura ) o di dolore
persistente dopo le terapie si passa a tecniche diverse ( mini
invasive o chirurgiche open ).Il tutto si può riassumere in questo
algoritmo che sintetizza le linee guida:

Fig. 7
Il Gruppo di studio SIOT precisa che:
L’asportazione chirurgica di una lesione metastatica scheletrica
solitaria può migliorare la sopravvivenza .Il trattamento delle
metastasi ossee richiede un approccio multidisciplinare da parte
dell’oncologo medico, del radioterapista e del chirurgo ortopedico, ma
i ruoli dei diversi specialisti devono essere coordinati allo scopo di
definire i tipi di terapia e la loro consecutio temporum per ottenere
un potenziamento che ne migliori l’efficacia.

 Laureato in Medicina e Chirurgia presso l'Università di Catania,
specializzato in Ortopedia e Traumatologia presso l'Università di Bologna
(Istituto Rizzoli) e specializzato in Fisiatria presso l'Università di Trieste.
Laureato in Medicina e Chirurgia presso l'Università di Catania,
specializzato in Ortopedia e Traumatologia presso l'Università di Bologna
(Istituto Rizzoli) e specializzato in Fisiatria presso l'Università di Trieste.


